





气相色谱质谱法(GC-MS)是一种将气相色谱(GC)与质谱(MS)联用的分析技术,以下是对该方法的详细解读:
原理
气相色谱分离原理:基于不同化合物在固定相和流动相之间的分配系数差异,当样品被载气带入色谱柱后,各组分在柱内的保留时间不同,从而实现分离。沸点低、极性小的化合物通常先出峰,沸点高、极性大的化合物后出峰。
质谱分析原理:使试样中各组分在离子源中发生电离,生成不同荷质比的带正电荷的离子,经加速电场的作用,形成离子束,进入质量分析器。在质量分析器中,再利用电场和磁场使离子发生相反的速度色散,将它们分别聚焦而得到质谱图,根据质谱图中的质荷比(m/z)和相对丰度等信息确定化合物的分子量、结构和组成等。
仪器构造
气相色谱部分:
进样系统:将样品引入气相色谱仪,常见的进样方式有手动进样、自动进样器等,可处理液体或气体样品。
色谱柱:核心部分,内壁涂有固定相,如硅胶或聚合物,样品在柱内因挥发性和亲和力不同而分离。
载气系统:载气如氦气、氮气或氢气,以一定流速推动样品在色谱柱中流动。
温控系统:精确控制色谱柱温度,优化分离效果。
检测器:监测色谱柱出口处样品组分的浓度,如氢火焰离子化检测器(FID)、电子捕获检测器(ECD)等。
质谱部分:
离子源:核心部件,将气态分子或气体样品转化为带电离子,常见的离子源有电子轰击电离源(EI)、化学电离源(CI)等。
质谱分析器:负责将带电离子根据质荷比(m/z)进行分离,常见的有四极杆质谱(QMS)、时间飞行质谱(TOF-MS)、离子阱质谱等。
质量检测器:测量经过分析器分离的离子的信号强度,并将信号转化为数据,质谱数据以质谱图形式呈现。
数据处理系统:用于控制仪器、采集数据以及进行数据处理和分析。
分析流程
样品制备:根据样品的性质和分析目的,选择合适的提取、净化和浓缩方法,将目标化合物从样品基质中分离出来。
进样:将处理后的样品通过进样系统引入气相色谱仪。
分离:样品在气相色谱柱中根据沸点、极性等差异进行分离,各组分按顺序从色谱柱流出进入质谱仪。
电离与碎裂:在质谱仪的离子源中,样品分子被电离成带正电荷的离子,并可能发生碎裂,形成一系列碎片离子。
质量分析与检测:离子进入质量分析器,根据质荷比进行分离和检测,质量检测器测量离子的信号强度。
数据处理与结果分析:计算机系统采集和处理质谱数据,通过与标准谱图比对、解析碎片离子等方式,对化合物进行定性鉴定和定量分析。
应用领域
环境分析:可用于监测水、空气、土壤中的污染物,如挥发性有机物、多环芳烃、农药残留等。
食品安全:检测食品中的农药残留、兽药残留、添加剂、毒素等有害物质,保障食品质量与安全。
药物分析:用于药物纯度检测、药物代谢产物分析、药物杂质鉴定等,为药物研发和质量控制提供支持。
石油化工:分析石油和天然气的成分,确定其组成和性质,指导石油加工和产品质量控制。
生命科学和生物技术:在蛋白质组学、代谢组学研究中,可用于分析生物样品中的小分子代谢物、脂质等。
发展趋势
高分辨率和高灵敏度:不断提高仪器的分辨率和灵敏度,能够检测到更低浓度和更复杂的化合物。
联用技术的发展:与其他分析技术如液相色谱、核磁共振等联用,实现更全面、深入的分析。
小型化和便携化:开发小型化、便携化的气相色谱质谱联用仪,便于现场分析和实时监测。
智能化和自动化:仪器操作更加智能化、自动化,数据处理和分析更加快速、准确,减少人工干预。
什么是气相色谱质谱法?
气相色谱质谱法(GC-MS)由两种截然不同的分析技术组成:气相色谱法(GC)与质谱法(MS)是连在一起的(因此使用连字符而非正斜线)。通常情况下,分析仪器由气相色谱仪组成,通过加热的传输线连接到质谱仪,这两种技术是串联进行的。然而,一些专业的、通常是微型的或便携式的仪器将整个GC-MS包含在一个盒子里。
气相色谱是一种分离科学技术,用于分离样品混合物中的化学成分,然后检测它们以确定其存在或不存在和/或存在多少。气相色谱检测器所提供的信息是有限的;这通常是二维的,即分析柱上的保留时间和检测器的反应。
鉴别的基础是将样品中的色谱峰的保留时间与使用相同方法分析的已知化合物标准的色谱峰进行比较。然而,单靠气相色谱不能用于鉴定未知化合物,这时与质谱的联用就非常有效。质谱可以作为唯一的检测器,也可以在质谱和气相色谱检测器之间分配色谱柱流出物。
质谱是一种测量带电粒子的质荷比(m/z)的分析技术,因此可用于确定分子量和元素组成,以及阐明分子的化学结构。GC-MS的数据是三维的,提供的质谱可用于确认身份或识别未知化合物,加上可用于定性和定量分析的色谱图。
GC-MS仪器是如何工作的?
在分析物分子被洗脱到质谱中进行检测之前,样品混合物首先被气相色谱分离[1]。它们由载气输送(图1(1)),载气不断流经气相色谱仪并进入质谱仪,在那里由真空系统抽空(6)。
有许多不同的质量分析器类型,这就是质量分辨率的巨大差异(因此仪器价格)。质量分辨率是指质量分析器分离m/z差异非常小的离子的能力。单位质量分辨率仪器只能分离名义质量或小数点后一位的质量,而高质量分辨率(HRMS)仪器可以分离到小数点后四或五位。
最常见的单位质量仪器是四极杆,它是一种扫描仪器,改变电压,只允许一定m/z的离子有稳定的轨迹通过四极杆,到达离子检测器。四极杆仪器有两种不同的操作模式:
离子阱也是一种扫描仪器,但它是三维的,在依次抛出离子到达离子检测器之前,将离子捕获在与质量有关的轨道上。
飞行时间(ToF)质量分析器根据离子沿飞行管到达离子检测器所需的时间来分离它们。在相同的动能下,质量较低的离子具有较高的速度,因此首先到达,而质量较高的离子具有较低的速度,较晚到达。
ToFMS仪器在质量分辨率和采集速率方面有不同的范围:非常快的ToFs,采集速率高达1000谱/秒,是单位质量分辨率,而HRMS ToFs的采集速率较低。高采集速率有利于二维气相色谱(GC × GC)的应用,峰宽低至30毫秒,然而HRMS对确定分子式非常有用。
因此,市场上有速度和质量分辨率不同的ToFs,选择哪种ToFs取决于应用,但GC的峰宽必须与MS的采集速率能力相匹配。
其他与GC连在一起的HRMS仪器包括磁区质量分析器,它利用电场和磁场弯曲离子的轨迹来分离它们。磁扇形GC-MS仪器在同位素比率分析中比较常见。
在HRMS orbitrap中,离子围绕一个中心转轴运行,它们在中心转轴上下移动的频率与m/z有关。
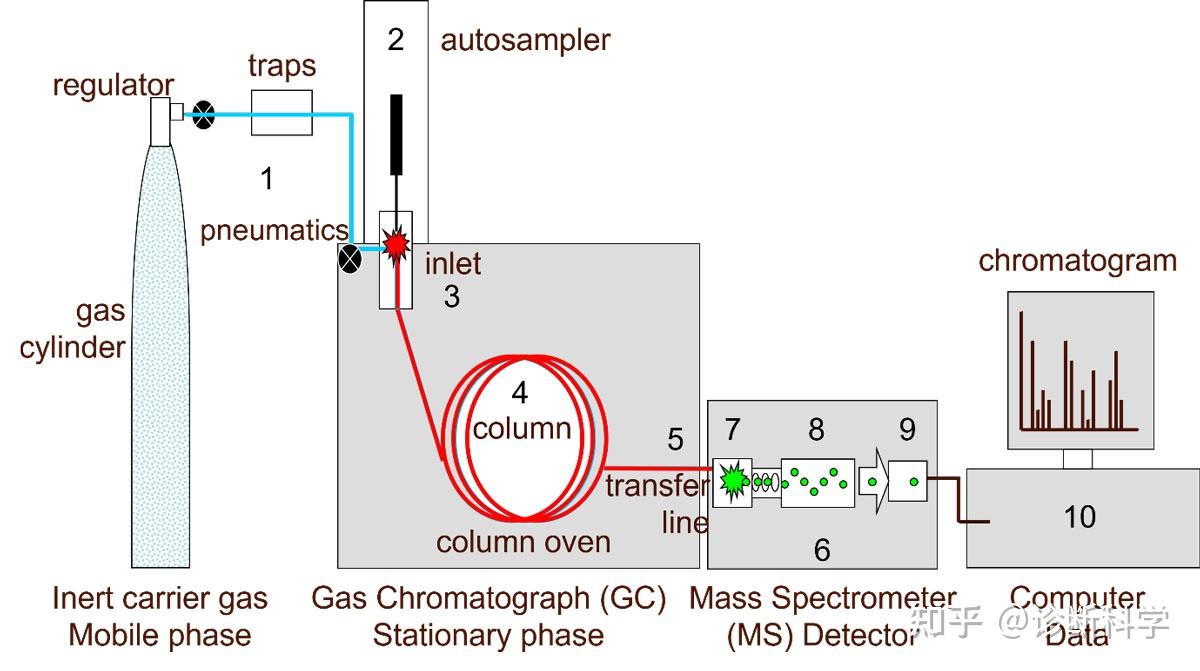
图1 | 气相色谱仪-质谱仪的简化图,显示(1)载气,(2)自动取样器,(3)进气口,(4)分析柱,(5)接口,(6)真空,(7)离子源,(8)质量分析器,(9)离子检测器和(10)电脑。
GC-MS分析和保留时间告诉你什么
GC-MS数据是三维的,如图2所示。X轴显示保留时间;从样品注入到GC运行结束的时间。这也可以看作是扫描数,也就是质谱在整个运行过程中获得的数据点的数量。y轴是离子检测器测量的反应或强度(图1(9))。z轴是所获得的质量范围内的离子的m/z。
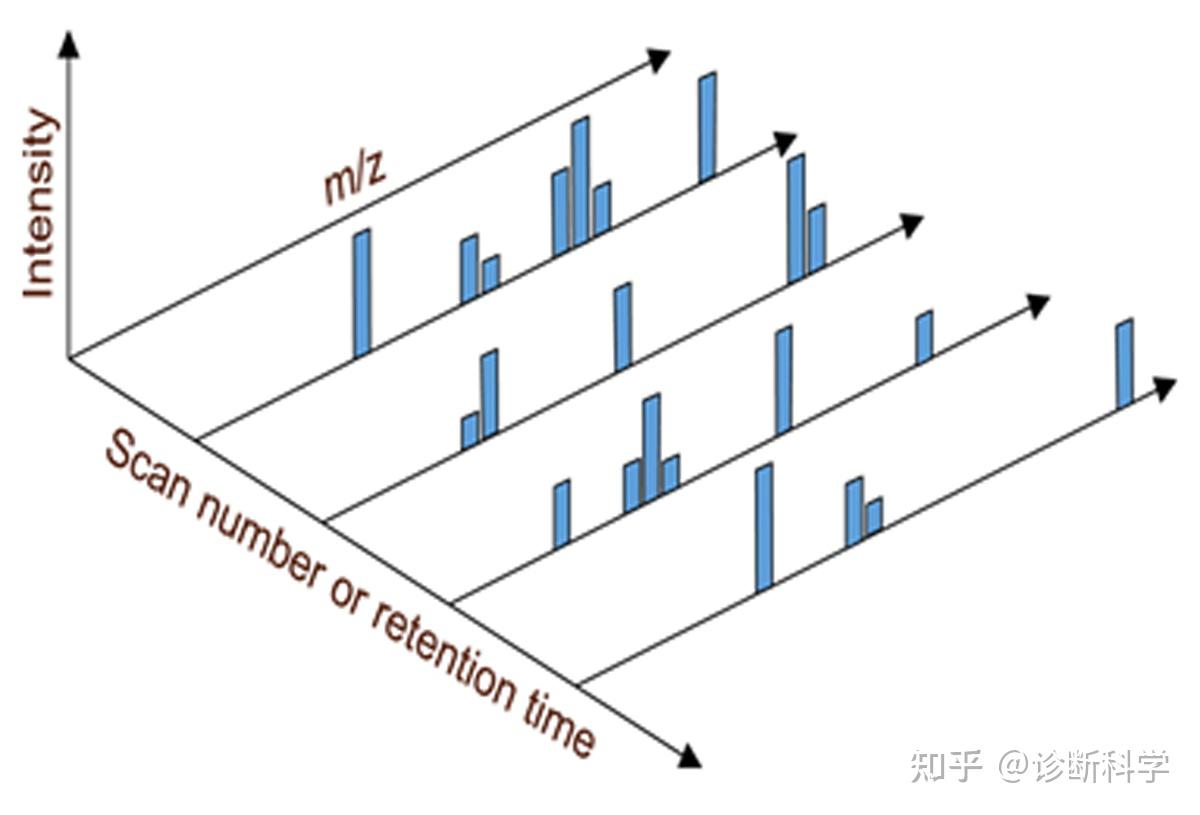
图2 | GC-MS数据是三维的,给出了扫描号/保留时间、响应/强度和m/z。
二维色谱图,如图3所示,是通过将单个数据点的所有离子丰度相加,并与保留时间(RT)/扫描号作图来产生总离子色谱图(TIC),这与GC检测器产生的色谱图更具可比性。然而,总离子色谱图中的每个数据点都是一个单独的质谱,通常可以在软件中的一个单独窗口中打开。在图3所示的例子中,峰3的顶点数据点已经被打开。
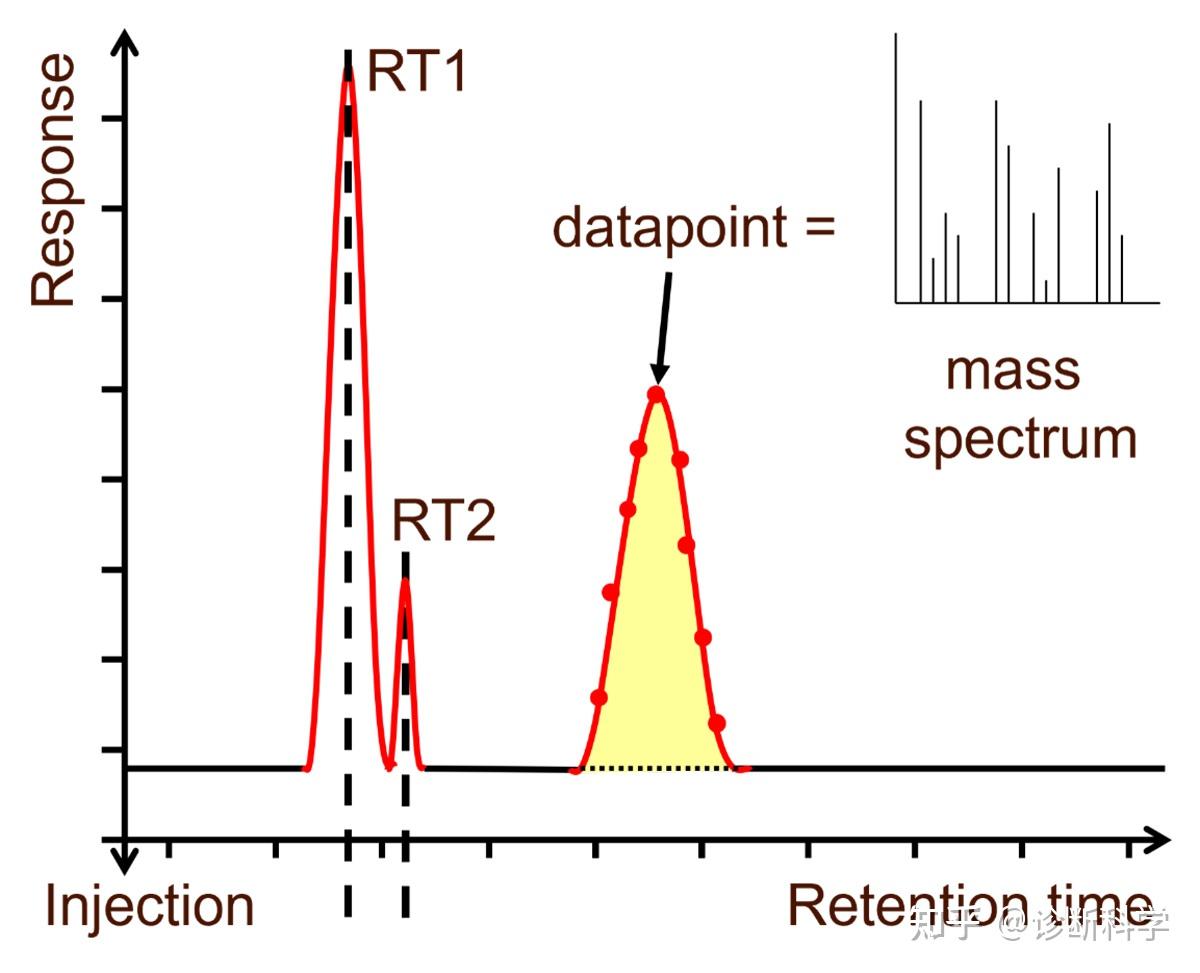
图3 | GC-MS输出的总离子色谱图(TIC)。
在图4中可以看到一个直链碳氢化合物正癸烷的质谱实例。在最右边可以看到分子离子142 m/z。由于癸烷是一种饱和碳氢化合物,电离产生的多余能量不能在内部脱域,因此大多数分子离子会发生碎片,导致许多碎片离子和分子离子的低丰度。饱和碳氢化合物的链长越长,分子离子的丰度越低,直到在质谱中观察不到分子离子。
然而,不饱和的分子离子,特别是那些有共轭双键的分子离子,如芳香族化合物,由于多余的能量可以更容易地内化,所以碎片较少。从癸烷的质谱中观察到的另一个现象是在m/z 43、57、71、85、99和113的一系列碎片离子,它们的m/z差异为14。
这些是由连续的-C2H4-单元的键的重叠裂解形成的,如果电荷是+1,这相当于28个统一的原子质量单位(u)的质量,是碳氢化合物的质谱的一个关键特征。质谱是分子的指纹,如果使用相同的电离技术和电压获得,可以与使用相同技术、相同电压获得的光谱库进行比较。
最常见的商业光谱库是在70eV下产生的EI光谱。质谱还可以通过离子的质量、同位素的存在和碎片离子之间的损失来解释,以确定分子式和分子的结构。
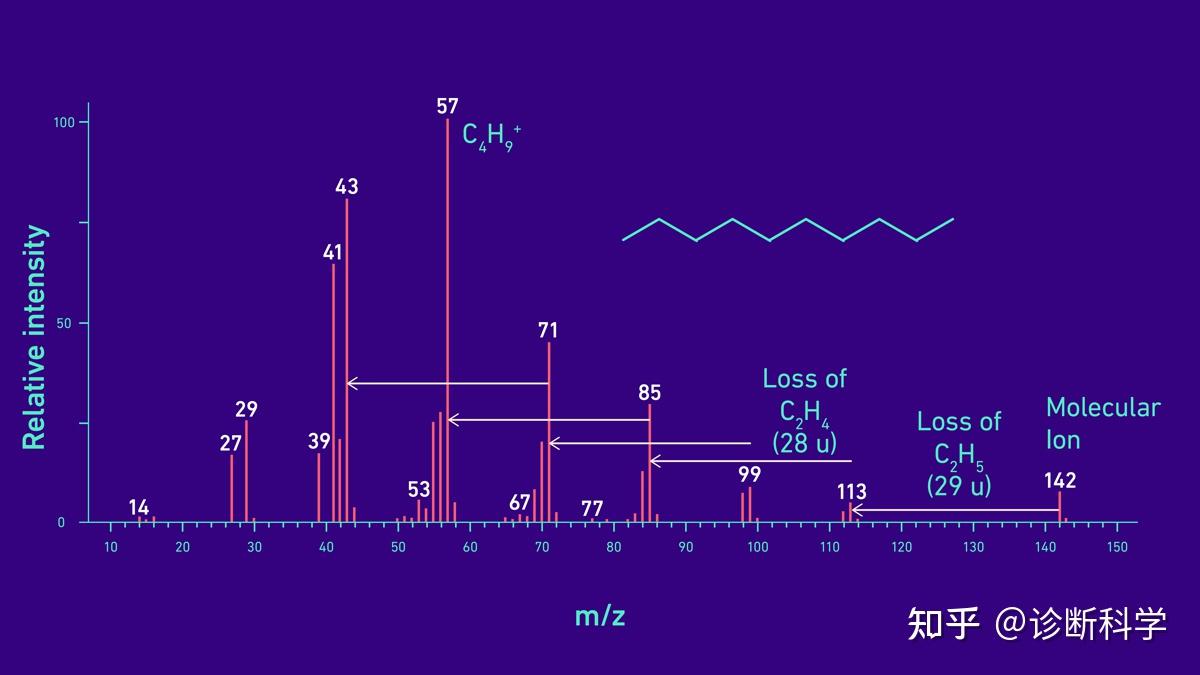
图4 | 直链碳氢化合物癸烷(C10H22)的质谱示例。
在GC中,保留时间用于识别目标分析物,通常面积用于定量。为了准确定量,色谱峰需要有良好的色谱分离和基线分辨率,如图3中RT1和RT2的色谱峰所示。对于GC-MS来说,质谱提供了一种额外的方法,可以使用完整的质谱或使用几个离子的存在和相对比例来确认目标分析物。使用GC-MS的数据进行定量,通常是根据单一的、独特的离子的面积,因为与使用TIC峰下的面积相比,它不太可能有来自共生峰的干扰。因此,只要能选择一个不存在于共混峰中的独特离子,从而使这些峰得到光谱解析,并能实现基线到基线的整合,就不需要色谱基线分辨率来进行准确定量。
GC-MS与GC-MS/MS
利用色谱和光谱分辨率对目标分析物的分离和鉴定是非常有力的。然而,在分析非常复杂的样品(如环境、食品或生物样品)中低至飞克(fg)水平的痕量分析物时,基质可能是难以承受的[2, 3]。样品制备可以用来去除大部分的基质;但是,分析物分子也经常丢失。
在色谱上,基质峰可以用GC×GC的方法从分析物峰中分离出来,即使用两个不同固定相的色谱柱。在质谱仪中,可以使用光谱分辨率,选择目标分析物的独特离子,这些离子不存在于共渗基质峰中。
然而,这在分析这些非常复杂的样品时经常失败,因为来自各种共混基质峰的碎片离子与来自目标峰的许多离子具有相同的m/z,扭曲了离子比率,导致错误的否定或不准确的定量。
串联质谱法(MS/MS)使用质谱仪内的多级(质量分析器),通过减少来自共混基质峰的背景来提高分析物的灵敏度。不同的、在色谱上共融的化合物可能会产生具有相同m/z的分子/碎片离子;但是,这些离子会有不同的结构。
电离后,第一个质量分析器选择离子,称为前体离子。下一阶段是将其进一步破碎,这通常是在惰性气体(如氩气)中通过一个称为碰撞诱导解离(CID)的过程实现的。产生的离子,称为产物离子,将取决于前体离子的结构,因此来自干扰物的产物离子质谱将与目标分析物的质谱不同。MS/MS的下一阶段是使用离子检测器之前的另一个质量分析器来分离产物离子。
有几种不同配置的MS/MS仪器,包括三重四极杆(QqQ),其中Q1用于前体选择,Q2用作碰撞池,Q3用作产物离子质量分析器。三重四极杆是最常见的,因为它们是单位质量的仪器,因此更实惠。图5是一个三重四极杆的例子,在多反应监测(MRM)模式下。Q-ToFs使用一个四极杆进行前体离子选择,一个HRMS ToF作为产物离子质量分析器。
离子阱能够进行MSn,所有阶段都发生在单个阱内。除了前体离子,所有的离子都被喷出,然后施加一个电压,与能量发生共振,使该特定m/z的前体离子失稳并产生碎片。然后这个过程可以重复进行,根据需要进行进一步的碎裂。
一般来说,MS/MS仪器只用于目标分析,不用于未知物的常规分析。有几种操作模式,包括MRM、单反应监测(SRM)(类似但更敏感)、产物离子扫描(Q3在扫描模式下操作以获得全部产物离子质谱)和中性损失扫描。
MS/MS仪器也可以作为标准质谱使用,这在MS/MS技术的方法开发过程中是需要的,然而,应该谨慎使用,因为产生的质谱可能质量较低,影响鉴定,特别是对于扫描仪器。一些制造商还启用了双采集模式,即在目标分析的MRM模式和识别未知物的扫描模式之间交替进行采集。
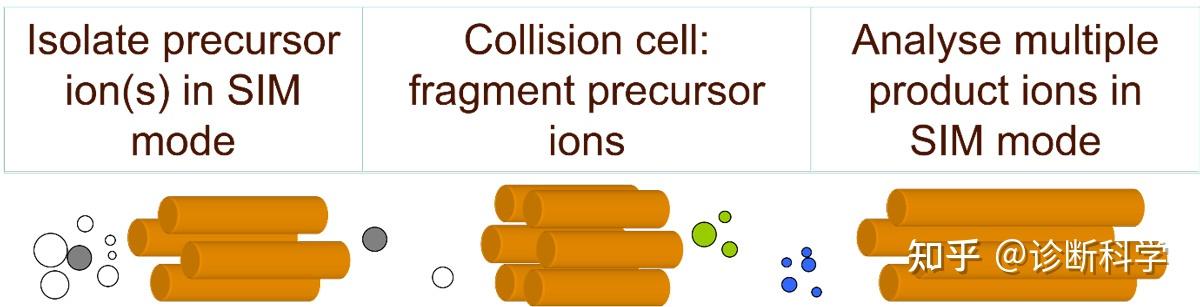
图5 | 三重四极杆MS/MS仪器在多反应监测(MRM)模式下的一个例子。
GC-MS的优势和局限
单独的GC是有局限性的,因为它不可能使用标准的GC检测器来识别未知的化合物,但是当与MS配对时,这是有可能的。相反,使用质谱直接分析样品会产生混合质谱,很难解构和解释,特别是当样品中有几个以上的化合物时。但与GC配对,就有了分离混合物的能力。
并非所有的化合物都能在标准气相色谱柱上分离,因此,使用光谱分辨率来消除干扰的能力导致了更准确的定量。质谱的解卷积能够检测基线和基质峰下的小峰,选择性的MS/MS能够在非常复杂的样品中识别微量分析物[4],而且干扰很少。
一种分析物的异构体通常具有相同或非常相似的质谱,因此仅用质谱就很难将它们区分开。因此,需要色谱分辨率来分离它们。各个异构体是通过其保留时间来识别的,为了准确的整合和定量,需要良好的色谱分辨率。
这对于同源系列也是如此,如饱和碳氢化合物,超过一定的链长,就看不到分子离子,质谱看起来都是一样的。同样,必须用保留时间来确定饱和碳氢化合物的身份。
就鉴定化合物时使用的分子离子的缺乏而言,可以使用替代的软化电离方法。例如,较低eV的电离或正负模式的化学电离可以导致较少的碎片离子,并防止分子离子的丢失或使其峰值更强。然而,碎片模式在很大程度上用于识别化合物的结构,通常需要建立目标库,因为软电离技术的目标库很少,但随着软电离技术的广泛使用,这种情况正在改善。
气相色谱和质谱的连用将两种强大的技术结合在一起,它们相互补充,可用于分离和鉴定样品中的化合物。当一种方法不能提供答案时,就可以依靠另一种方法。
GC-MS的常见问题
GC-MS仪器中最常见的问题是泄漏到系统中和系统污染。
质谱仪通常有真空,以减少背景干扰和离子-分子反应,增加部件的使用寿命,减少维护,并避免任何放电,因为质谱仪内使用高电压。要获得良好的灵敏度需要非常好的真空,小的泄漏会增加背景,而大的泄漏会阻碍真空系统的运行。
高柱流增加了进入质谱的气体分子的数量,而真空系统不能足够快地抽空它们以建立良好的真空,因此灵敏度降低。因此,当把一个方法从GC转移到GC-MS时,应该使用较小的内径柱子和较低的柱流量。高灵敏度分析的最大流速取决于质谱仪的真空系统。为了获得最佳的分离效率,应该了解并考虑到这一点,以及载气的最佳流速。
质谱仪是敏感的仪器,需要定期维护,清洁离子源和更换真空泵中的油,以保持良好的灵敏度。来自样品的高分子量基质应保留在气相色谱仪的进气口衬垫中,通过优化进气口温度,使其易于更换,而不是转移到色谱柱中,因为它可能损坏固定相并弄脏质谱离子源。
离子源污染的另一个来源是色谱柱渗漏。应该在质谱仪中安装更稳定的“-MS”柱,并且在连接到质谱仪时不应该进行柱的调节。
与GC有关的问题仍然会发生,例如活性和样品降解,特别是在样品经过较少的样品制备的情况下,例如使用GC-MS/MS,基质不能被“看见”。
GC-MS和GC-MS药物检测的应用
GC-MS和GC-MS/MS被用于许多行业的常规分析,寻找分子量通常小于700 amu的挥发性污染物,例如在食品[2]、环境[5]、法医[6]、反兴奋剂[7]和消费品[8]行业。GC-MS也被用于研究,以确定未知的挥发性化合物,包括在食品和香料、空间、石油化工、化学、农业、烟草、制药、医疗保健、能源、采矿、环境和法医等领域,仅举几例。
以药物检测为例,可以出于多种原因进行检测:病理学、保健和人与动物的反兴奋剂[9]。像尿液和血样这样的生物液体是复杂的,有大量的基质,而且通常药物的浓度很低。
因此,对它们的检测需要像GC-MS这样的联用技术,以开始将目标或感兴趣的化合物从基质峰中分离出来。然后可以用MS/MS和更经常使用的MS/MS与HRMS,有时是额外的GC x GC分离来选择性地识别它们。
诊断科学编辑团队收集、整理和编撰,如需更多资讯,请关注公众号诊断科学(DiagnosticsScience)。
参考文献
评论